Η Χρόνια Νεφρική Νόσος (ΧΝΝ) εξελίσσεται και επιδεινώνεται: Πώς?
Ιωάννης Γ. Γριβέας
Νεφρολόγος, Διευθυντής Νεφρολογικού Τμήματος 401 ΓΣΝΑ
Η ΧΝΝ εξελίσσεται μέσω 3 φάσεων: α) μία αρχική «εισβολή» ενός «τοξικού» παράγοντα προκαλεί, β) την ενεργοποιήση μηχανισμών «επιδιόρθωσης» της βλάβης που δημιουργείται, οι οποίοι μηχανισμοί πολλές φορές όχι μόνο δεν βοηθούν αλλά προκαλούν και περαιτέρω επιδείνωση της νεφρικής λειτουργίας. Όσο περισσότεροι νεφρώνες χάνονται γ) οι υπόλοιποι αντιδρούν στην επηρεασμένη συνολικά νεφρική λειτουργία με αλλαγές στον τρόπο λειτουργίας τους, οι οποίες μπορεί να αποδειχθούν καθοριστικές για την επιβίωση των εναπομείναντων νεφρώνων. Οι τρείς παραπάνω φάσεις μπορεί να καλύπτουν η μία την άλλη χρονικά κατά διαστήματα, οι μηχανισμοί τους όμως είναι απόλυτα διακριτοί. Είναι γνωστό ότι όταν ένας ασθενής εμφανιστεί με ΧΝΝ, το πρωτοπαθές αίτιο δεν είναι πάντοτε σαφές. Αυτό που έχει όμως πραγματική σημασία παθοφυσιολογικά είναι η διαδικασία της συνεχούς εξέλιξης της ΧΝΝ.
Ανοίγοντας μία παρένθεση, για να συνδέσουμε τη φυσιολογία με τη σύγχρονη κλινική πράξη και παρατήρηση είναι σωστό να τονιστεί ότι μέχρι σήμερα υπάρχει περιορισμένος αριθμός προοπτικών μελετών παρατήρησης ειδικά σχεδιασμένων ώστε να εστιάζουν στη φυσική εξέλιξη της ΧΝΝ. Πέραν του περιορισμένου αριθμού τους, παρουσιάζουν αισθητές διαφορές στα κριτήρια ένταξης των ασθενών, στις πληροφορίες που συλλέγονται και στον τρόπο που αξιολογούνται τα όποια αποτελέσματα. Οι κύριοι στόχοι των διαφόρων μελετών μπορούν να συνοψιστούν στη σχέση ΧΝΝ με την καρδιαγγειακή νόσο, στην περιγραφή εξέλιξης της ΧΝΝ, στην αναγνώριση πιθανών παραγόντων κινδύνου και στο ρόλο της οστικής νόσου σε στάδια ΧΝΝ πριν την ένταξη σε πρόγραμμα περιοδικής αιμοκάθαρσης.
Μέχρι σήμερα δεν υπάρχουν μελέτες με εστίαση σε υψηλού κινδύνου ασθενείς με ΧΝΝ, ως αποτέλεσμα του ρυθμού επιδείνωσης νεφρικής λειτουργίας με ή χωρίς λευκωματουρία. Οι περισσότερες μελέτες εστιάζουν στο στάδιο της ΧΝΝ. Υπάρχει όμως μία βασική διαφορά, ενώ το στάδιο της ΧΝΝ από μόνο του ορίζει ένα βαθμό κινδύνου, μεγαλύτερη προγνωστική αξία φαίνεται να έχει ο ρυθμός επιδείνωσης της νεφρικής λειτουργίας με την παρουσία ή όχι λευκωματουρίας.
Μελετητές έχουν παρατηρήσει ότι ο ρυθμός επιδείνωσης της νεφρικής λειτουργίας είναι μάλλον γραμμικός (linear) (Εικ. 1). Η παρατήρηση αυτή στην πράξη σημαίνει ότι υπάρχει ένα βιολογικό μονοπάτι διαμέσου του οποίου η απώλεια της νεφρικής λειτουργίας είναι αναπόφευκτη.
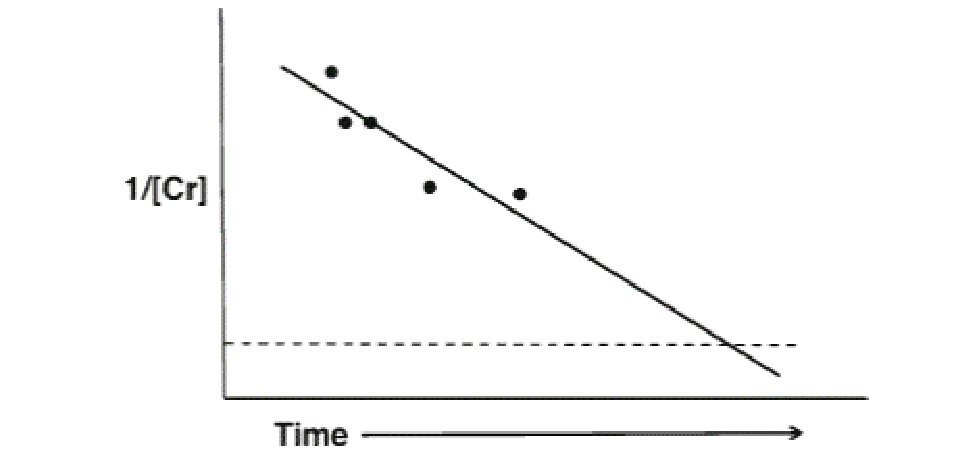
Εικόνα 1: Η απώλεια της νεφρικής λειτουργίας έχει γραμμικό χαρακτήρα καθώς η ΧΝΝ εξελίσσεται (δεδομένα από το άρθρο Schnaper HW. Remnant nephron physiology and the progression of chronic kidney disease. Pediatr Nephrol 2014;29:193-202)
Όλα μάλιστα τα γεγονότα τα οποία επηρεάζουν ή εμπλέκονται στο μονοπάτι αυτό αναπαραγάγουν τον ίδιο φαύλο κύκλο της νεφρικής ανεπάρκειας. Η απάντηση στη νεφρική επιδείνωση διαμέσου υπερδιήθησης και υπερτροφίας των υπόλοιπων λειτουργώντων νεφρώνων οδηγεί σε περαιτέρω επιδείνωση της νεφρικής λειτουργίας.
Η πολυπλοκότητα της νεφρικής λειτουργίας υποστηρίζει τη θεωρία ότι καθώς η ΧΝΝ εξελίσσεται διάφορες δυνάμεις, εντός και εκτός νεφρού, με αντίρροπες δράσεις επηρεάζουν το ρυθμό επιδείνωσης. Η βασική αρχή είναι η διατήρηση της ομοιόστασης του οργανισμού, δηλαδή καθώς τμήμα του νεφρικού ιστού χάνει τη λειτουργικότητα του, ορμονικοί μηχανισμοί «φορτώνουν» με περισσότερο έργο τον υπόλοιπο νεφρικό ιστό. Σε επίπεδο του κάθε μεμονωμένου νεφρώνα η στενή ανατομική σχέση μεταξύ σπειραματικού και σωληναριακού αγγειακού δικτύου, υποστηρίζει τη διατήρηση της σπειραματοσωληναριακής ισορροπίας μέσω της οποίας η διήθηση και η επαναρρόφηση συνδέονται άρρηκτα, παρατήρηση η οποία θα μας χρειαστεί αργότερα.
Απώλεια νεφρώνων στην παθογένεση της ουραιμίας Μία απλή και κατατοπιστική εικόνα (Εικ. 2) για το πώς η επιδίωξη για διατήρηση αυτής της ισορροπίας οδηγεί στην εγκατάσταση της ουραιμικής συνδρομής έχει προταθεί από τους Bricker και συν.7,8. Mετά από ένα διάστημα, οι νεφρώνες από το νεφρό που συνεχίζουν να λειτουργούν, αφού έχουν υπερτραφεί, αδυνατούν να «υποκαταστήσουν» περαιτέρω την απώλεια νεφρώνων και ο ρυθμός σπειραματικής διήθησης προοδευτικά αρχίζει να μειώνεται. Σε ένα πιο προχωρημένο στάδιο, τα αυξημένα επίπεδα φωσφόρου (PO43-) και τα ελαττωμένα ασβεστίου (Ca2+) ενεργοποιούν την αύξηση της παραθορμόνης (PTH), η οποία με τη σειρά της επαναφέρει τα επίπεδα Ca2+ και PO43- εντός φυσιολογικών ορίων. Αυτό βέβαια ισχύει μέχρι να εξαντληθεί η ικανότητα των νεφρώνων να αποβάλλουν PO43-, γιατί μετά το PO43- και η PTH παραμένουν υψηλά και το Ca2+ χαμηλά. To αξιοσημείωτο είναι ότι η «λειτουργούσα» νεφρική μάζα προοδευτικά δεν μπορεί να υλοποιήσει την ομοιόσταση του οργανισμού, αλλά τα ορμονικά σήματα συνεχίζουν να εκπέμπονται με αρνητικές συνέπειες όμως τόσο για το νεφρό, όσο και για όλο τον οργανισμό.
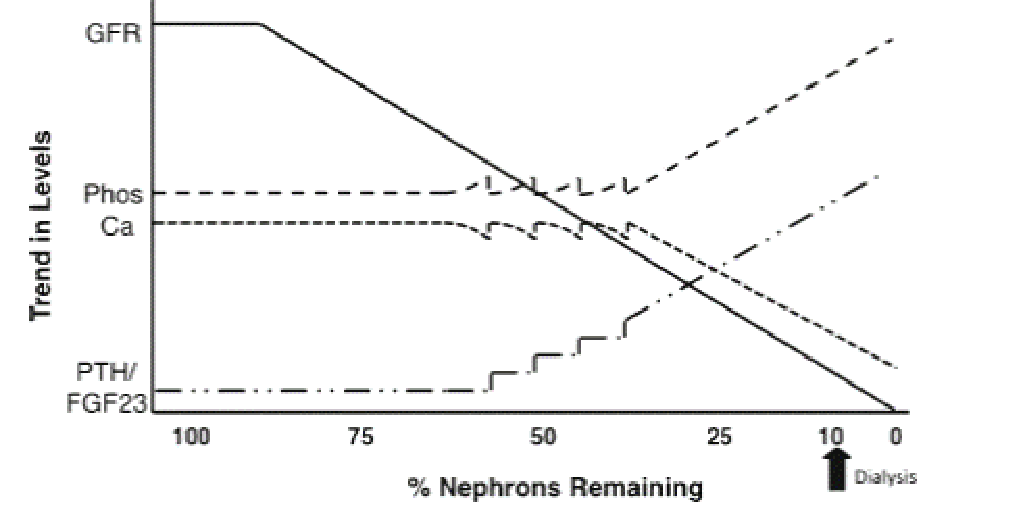
Εικόνα 2: Μετά από ένα διάστημα, οι νεφρώνες από το νεφρό που συνεχίζουν να λειτουργούν, αφού έχουν υπερτραφεί, αδυνατούν να «υποκαταστήσουν» περαιτέρω την απώλεια νεφρώνων και ο ρυθμός σπειραματικής διήθησης προοδευτικά αρχίζει να μειώνεται. Αυτό έχει ως συνέπεια την διαταραχή του ισοζυγίου των επιπέδων Ca2+, PO43- και PTH. (δεδομένα από το άρθρο Bricker NS. On the pathogenesis of the uremic state. An exposition of the “trade-off hypothesis”. N Engl J Med 1972; 286:1093–1099).
Δομικές αλλαγές Έχει αναφερθεί ότι η απώλεια νεφρώνων είναι αποτέλεσμα της αρχικής «εισβολής» ενός «τοξικού» παράγοντα. Αυτός ο παράγοντας μπορεί να στοχεύσει, είτε στο σπείραμα, είτε στο σωληνάριο. Η σπειραματική βλάβη μπορεί να αρχίσει και να εξελιχθεί στη βάση φλεγμονής, θρομβογένεσης, πρωτοπαθούς δυσλειτουργίας του ποδοκυττάρου, αγγειακής βλάβης ή και συνδυασμού όλων των παραπάνω παραγόντων, όπως συμβαίνει στο συστηματικό ερυθηματώδη λύκο. Πολλοί μηχανισμοί έχουν προταθεί για το πώς ο παραπάνω «τραυματισμός» μπορεί να προκαλέσει απώλεια νεφρώνων. Μία πιθανή θεωρία θέλει την απώλεια του ποδοκυττάρου να οδηγεί στην απογύμνωση του σπειράματος από τριχοειδή, τη δημιουργία συμφύσεων του ενδοθηλίου με την κάψα του Bowman, η οποία με τη σειρά της επιτρέπει την έξοδο των πρωτεϊνών του πλάσματος στον περισπειραματικό χώρο, με τελικό αποτέλεσμα την φλεγμονή και την ινωδογένεση.
Εναλλακτικά η βλάβη μπορεί να αρχίσει από το σωληνάριο ή το διάμεσο χώρο. Τραυματισμός των σωληναριακών κυττάρων ισχαιμικής, τοξικής ή φλεγμονώδους αιτιολογίας σε βαθμό που δε μπορούν να αναγεννηθούν είναι το πιο συνηθισμένο σενάριο. Σ’ αυτή την περίπτωση τα σπειράματα συνιστούν μεταβατικές μορφές μέχρι την πλήρη απώλεια των νεφρώνων.
Yπερτροφία των νεφρώνων ως παράγοντας επιδείνωσης της ΧΝΝ Σ’ αυτό το «παιχνίδι» εξελισσόμενης απώλειας νεφρώνων, οι υπόλοιποι λειτουργούντες νεφρώνες πρέπει για να ανταποκριθούν στο έργο τους, είτε να αυξήσουν την δραστηριότητα τους, είτε τη μάζα τους. Σε πειραματική μοντέλα με ετερόπλευρη νεφρεκτομή η υπερδιήθηση των λειτουργόντων σπειραμάτων αρχίζει μέσα σε ώρες. Βασικός μεσολαβητής της παραπάνω διαδικασίας είναι το σύστημα ρενίνης-αγγειοτενσίνης, το οποίο ρυθμίζει τόσο την αιμοδυναμική του φαινομένου, όσο και την αντιδραστική κυτταρική υπερτροφία και υπερπλασία. Η αυξημένη σπειραματική διήθηση πρωτεϊνών του πλάσματος οδηγεί σε διαμεσοσωληναριακή βλάβη. Μία σειρά από εξηγήσεις έχουν δοθεί για το παραπάνω φαινόμενο, συμπεριλαμβανομένης και της ύπαρξης στην περιοχή βιολογικά δραστικών ουσιών που προκαλούν φλεγμονή και οξείδωση. Σε κάθε περίπτωση, είτε πρόκειται για σπειραματική, είτε για σωληναριακή βλάβη η ΧΝΝ εξελίσσεται διαμέσου της υπερτροφίας των νεφρώνων που περιλαμβάνει ένα κύκλο κυτταρικής διαφοροποίησης, φλεγμονής, ενδοθηλιακής δυσλειτουργίας, αυξημένων μεταβολικών αναγκών, ιστικής υποξίας και οξέωσης. Όλες οι παραπάνω απαντήσεις στην απώλεια λειτουργικών νεφρώνων συμβάλλουν η καθεμία με τον τρόπο της στην εξέλιξη της ΧΝΝ.
ΒΙΒΛΙΟΓΡΑΦΙΑ
- Schnaper HW. Remnant nephron physiology and the progression of chronic kidney disease. Pediatr Nephrol 2014; 29: 193-202.
- Stephanie Stringer, Praveen Sharma, Mary Dutton, et al. The natural history of, and risk factors for progressive Chronic Kidney Disease (CKD): the Renal Impairment in Secondary care (RIISC) study; rationale and protocol. BMC Nephrology 2013; 14: 95.
- Γριβέας Ι. Χρόνια Νεφρική Νόσος: Από την πρωτοβάθμια στην δευτεροβάθμια φροντίδα. Ελληνική Νεφρολογία 2014; 26(4): 303-309.
- Shlipak MG, Katz R, Kestenbaum B, et al. Rapid Decline of Kidney Function Increases Cardiovascular Risk in the Elderly. J Am Soc Nephrol 2009; 20: 2625-26
- Bricker NS. On the pathogenesis of the uremic state. An exposition of the “trade-off hypothesis”. N Engl J Med 1972; 286: 1093-1099.
- Bricker NS, Fine LG, Kaplan M, Epstein M, Bourgoignie JJ, Light A. “Magnification phenomenon” in chronic renal disease. N Engl J Med 1978; 299: 1287-
- Marcussen N. A tubular glomeruli and the structural basis for chronic renal failure. Lab Invest 1992; 66: 265-284.
10. Komers R, Meyer TW, Anderson S. Pathophysiology and nephron adaptation in chronic kidney disease. In: Coffman TM, Falk RJ, Molitoris BM, Neilson EG et al (eds) Schrier’s diseases of the kidney and urinary tract, 2013; 9th edition. Lippincott Williams & Wilkins, Philadelphia, p.p. 2214-2237.